تایید داروی توفاسیتینیب برای آرتریت پسوریاتیک فعال
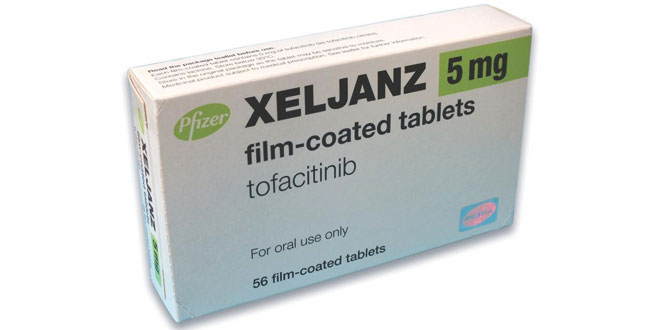
تایید داروی توفاسیتینیب برای آرتریت پسوریاتیک فعال
سازمان غذا و داروی آمریکا چراغ سبز خود را به روی توفاسیتینیب tofacitinib با نام تجاری Xeljanz/Xeljanz XR و محصولی از Pfizer روشن کرد. این دارو برای درمان بزرگسالان مبتلا به آرتریت پسوریاتیک فعال (PsA) که به متوتروکسات یا دیگر داروهای آنتیروماتیک تعدیل کننده بیماری (DMARDs) پاسخ کافی درمانی نمیدهند یا آنها را تحمل نمیکنند، تائید شده است.
توفاسیتینیب نوعی مهارکننده JAK خوراکی است که در سیگنالدهی سیتوکینهای متعددی که در پاسخدهی ایمنی دخیل هستند، تداخل ایجاد میکند. این دارو برای نخستین بار در سال ۲۰۱۲ برای درمان بزرگسالان مبتلا به آرتریت روماتوئید فعال با شدت متوسط تا شدید که پاسخ درمانی کافی به متوتروکسات نمیدهند یا نمیتوانند آن را تحمل کنند، توسط FDA تائید شده است.
دادههای به دست آمده از برنامه ارتقای بالینی فاز ۳ Oral Psoriatic Arthritis Trial که شامل دو مطالعه OPAL Broaden و OPAL Beyond است، همچنین یک مطالعه طولانیمدت در حال انجام، با نام OPAL Balance به تائید این دارو انجامیده است.
یافتههای OPAL Broaden و OPAL Beyond در اکتبر ۲۰۱۷ در New England Journal of Medicine منتشر شدهاند.
هر دوی این مطالعات نشان دادند که بهبود قابل توجه و معنیداری در پاسخ ACR20 و تغییر نسبت به پایه در نمره شاخص Health Assessment Questionnaire–Disability Index طی ۳ ماه درمان در بیماران دریافت کننده Xeljanz 5 میلیگرمی، دو بار در روز در ترکیب با یک DMARD غیربیولوژیک، در مقایسه با پلاسبو، ایجاد میشود.
شایعترین عوارض جانبی که در بیش از ۳ درصد بیماران دریافت کننده Xeljanz دیده شد، عبارت بودند از نازوفارنژیت، عفونت دستگاه تنفسی فوقانی، سردرد و اسهال.
برچسب اطلاعات دارویی توفاسیتینیب دربرگیرنده هشداری است مبنی بر احتمال افزایش خطر ابتلا به عفونتهای جدی که ممکن است منجر به بستری در بیمارستان یا مرگ بیمار میشود. بسیاری از بیمارانی که به این عفونتها مبتلا شدند، همزمان داروهای ایمونوساپرسیو دیگری هم دریافت میکردند، مانند متوتروکسات یا کورتیکواستروئیدها. اگر عفونتهای جدی رخ دهد، مصرف توفاسیتینیب باید تا زمان کنترل عفونت قطع شود.